PRISE EN CHARGE D’UNE COLITE A Clostridium difficile en 2019

BULLETIN INFO n° 30
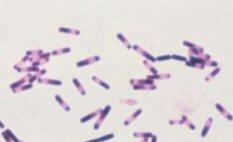
Clostridium difficile (CD) est une bactérie, bacille à Gram positif anaérobie stricte et sporulée ce qui lui confère une grande résistance dans le milieu extérieur.
Cette bactérie peut produire des toxines (toxine A et toxine B) qui vont agir au niveau de la muqueuse intestinale à l’origine de la symptomatologie.
Cette bactérie est à l’origine de 15 à 25% des colites post antibiotiques, de plus de 95% des colites pseudomembraneuses et est la principale cause des diarrhées nosocomiales.
Les principaux facteurs de risque de colite à Clostridium difficile (CCD) sont la prise d’antibiotiques dont certains avec une plus grande fréquence (tableau 1), l’âge au-delà de 65 ans, les antécédents d’hospitalisation, les traitements modifiant le microbiote intestinal et les maladies inflammatoires chroniques de l’intestin (MICI).
La transmission est interhumaine, le plus souvent par manuportage mais également par l’environnement contaminé et certains hôtes animaux (porcs).
Seules les souches de Clostridium difficile toxinogènes sont pathogènes. On décrit deux manifestations digestives distinctes :
- la diarrhée post-antibiotiques « simple » qui se traduit par une diarrhée fécale sans glaires ni sang et sans altération de l’état général, une fièvre modérée peut être fréquente.
- la colite pseudomembraneuse dont le tableau plus marqué se traduit par une diarrhée liquide abondante souvent non sanglante avec fièvre et douleurs abdominales. Le bilan biologique sanguin montre alors une hyperleucocytose avec élévation de la CRP. Les complications de la colite pseudomembraneuse sont le choc septique et le mégacôlon toxique pouvant entrainer une perforation colique.
Les CCD sont caractérisées par un taux élevé de récidives qui surviennent généralement 8 semaines après un épisode résolutif traité.
Le ribotype 027 (variant hypervirulent) à l’origine d’infections sévères et épidémiques semble actuellement en diminution.
Diagnostic
L’association d’un tableau clinique compatible et la présence d’une souche de Clostridium difficile toxinogène posent le diagnostic. Cette recherche fait appel à la détection couplée d’une enzyme de la bactérie associée à la présence de toxine recherchée soit par test immunochromatographique soit par amplification des acides nucléiques.
Cette recherche est effectuée quotidiennement sur notre plateau technique et le résultat est rendu dans les deux heures après réception du prélèvement de selles.
Traitement d’une CCD
Il repose sur des mesures générales :
– Arrêt ou modification du traitement antibiotique responsable de l’épisode
– Arrêt de tout traitement ralentisseur du transit
– Ré équilibration hydro-électrolytique
Et sur des mesures spécifiques et notamment une antibiothérapie ciblée:
– Vancomycine per os 125mg 4x/j pendant 10j pour les formes non sévères (la dose de 2g/j est recommandé en cas de forme fulminante).
– ou Fidaxomicine 200mg 2x/j pendant 10j (mais coût élevé)
Il faut signaler que ces 2 molécules ne sont délivrées que par les pharmacies hospitalières à partir d’une ordonnance rédigée par un médecin hospitalier
– Le Métronidazole 500mg 4x/j pendant 10j utilisé jusqu’alors n’est plus recommandé en première intention en raison d’une moindre sensibilité et d’une destruction du microbiote intestinal. On réserve son utilisation en cas de contre-indication à la vancomycine ou à la fidaxomicine.
Traitement d’une récidive de CCD
Il repose en général sur un traitement n’ayant pas été utilisé en première intention :
– soit Fidaxomicine 200mg 2x/j pendant 10j
– soit Vancomycine à dose décroissante (pleine dose pendant 2 semaines puis diminution de 250mg par semaine)
Prévention des récidives de CCD
– Elle fait appel à la transplantation de microbiote fécal à partir de la 3ème récidive et après échec du traitement antibiotique (vancomycine ou fidaxomicine).
Tableau 1 : Classes d’antibiotiques et leur association aux CCD
Pierre Hance